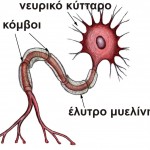
Πρόκειται για μία νόσο του ΚΝΣ που οφείλεται στην καταστροφή της
μυελίνης που περιβάλλει τους νευράξονες (άξονες των νευρικών κυττάρων
μέσω των οποίων μεταδίδεται η πληροφορία σε ένα άλλο κύτταρο) (Πηγή 1).
Η βαρύτητα και η κλινική πορεία της νόσου διαφέρουν σημαντικά από ασθενή σε ασθενή.
Η θεραπευτική αγωγή βασίζεται κυρίως σε ανοσοκατασταλτικά - ανοσοτροποποιητικά φάρμακα, ψυχολογική υποστήριξη και φυσική αποκατάσταση.
Αιτιολογία
Η αιτιολογία της νόσου είναι άγνωστη. Τα έως τώρα επιστημονικά δεδομένα οδηγούν στο συμπέρασμα ότι πρόκειται για μια διαταραχή του ανοσοποιητικού συστήματος το οποίο πιθανόν αντιδρά ανώμαλα στην προσπάθειά του να εξουδετερώσει κάποιον εξωτερικό παράγοντα.
Πιθανολογείται ότι ο παράγοντας αυτός είναι ένας ή περισσότεροι ιοί.
Παθογένεια
Πρόκειται για μια αυτοάνοση διαταραχή που έχει σαν τελικό αποτέλεσμα την δημιουργία αντισωμάτων ενάντια στην βασική πρωτεΐνη της μυελίνης του ΚΝΣ.
Τα αυτοαντισώματα αυτά δεν καταστρέφουν το σύνολο της μυελίνης του ΚΝΣ αλλά συγκεκριμένες περιοχές κάθε φορά, οι οποίες ονομάζονται εστίες ή πλάκες απομυελίνωσης.
Δεδομένου ότι η μυελίνη στο ΚΝΣ παίζει ουσιαστικό ρόλο στην μετάδοση της πληροφορίας από τον ένα νευρώνα στον άλλο (Πηγή 1), η καταστροφή της προκαλεί διακοπή της επικοινωνίας των διαφόρων τμημάτων του ΚΝΣ με αποτέλεσμα την δυσχερή λειτουργία του.
Κλινική εικόνα - Συμπτώματα
Η συμπτωματολογία της ΣΚΠ (σκλήρυνσης κατά πλάκας) διαφέρει από ασθενή σε ασθενή, αλλά μπορεί να διαφέρει και από ώση σε ώση του ίδιου ασθενούς.
Εξαρτάται από την περιοχή όπου προέκυψε η εστιακή βλάβη της μυελίνης.
Π.χ. αν η βλάβη αυτή αφορά τις αισθητικές οδούς, η συμπτωματολογία θα είναι αιμωδίες (μουδιάσματα), παραισθησίες (μυρμηγκιάσματα). Αν αφορά τις κινητικές οδούς τότε θα έχουμε σαν αποτέλεσμα μείωση ή κατάργηση της μυϊκής ισχύος του ασθενούς (πάρεση ή παράλυση).
Βέβαια, η βλάβη μπορεί να αφορά και οποιαδήποτε άλλη ανατομική δομή του ΚΝΣ με συμπτωματολογία ανάλογη της λειτουργίας του κάθε ανατομικού σχηματισμού. Π.χ. αν η βλάβη αφορά την παρεγκεφαλίδα τότε θα έχουμε δυσαρθρία, αστάθεια βάδισης, ασυνεργία κινήσεων κ.α.
Επίσης, η κλινική εικόνα μπορεί να διαφέρει από ασθενή σε ασθενή. Διακρίνουμε τις περιπτώσεις όπου η νόσος εξελίσσεται με ώσεις ενώ στα μεσοδιαστήματα ο ασθενής είναι φαινομενικά υγιής. Αντίθετα σε άλλες περιπτώσεις εγκαθίσταται μία συμπτωματολογία η οποία επιδεινώνεται με το πέρασμα του χρόνου (προϊούσα μορφή).
Τέλος, συχνή είναι η προσβολή του οπτικού νεύρου με αποτέλεσμα θάμβος οράσεως (οπισθοβολική νευρίτις).
Διάγνωση
Βέβαια, ένας ασθενής που περιγράφει ένα ή περισσότερα από τα ανωτέρω συμπτώματα δεν πάσχει αναγκαστικά από ΣΚΠ. Η συμπτωματολογία εστιακής βλάβης του ΚΝΣ μπορεί να οφείλεται σε διάφορες άλλες αιτίες που προκαλούν βλάβη σε κάποιο σημείο του ΚΝΣ.
Μερικά από αυτά τα αίτια είναι: όγκοι, αγγειακά επεισόδια, αποστήματα, φλεγμονώδεις παθήσεις και απομυελινώσεις άλλης αιτιολογίας.
Επίσης, μπορεί το αναφερόμενο σύμπτωμα να οφείλεται σε άλλου είδους διαταραχή και όχι σε εστιακή βλάβη.
Π.χ. ένας ασθενής που αναφέρει αιμωδίες άνω άκρων μπορεί να πάσχει από νευροφυτικές διαταραχές, σύνδρομο καρπιαίου σωλήνα, περιφερική νευροπάθεια κ.α.
Για τον λόγο αυτό η διάγνωση της ΣΚΠ τίθεται από ειδικούς γιατρούς (Νευρολόγους) με βάση συγκεκριμένα κριτήρια τα οποία είναι κατ' εξοχήν κλινικά (χρησιμοποιούνται ευρέως τα κριτήρια του Poser)( Πηγή 4) αλλά και εργαστηριακά (κυρίως Μαγνητική Τομογραφία Εγκεφάλου ή Σπονδυλικής Στήλης ( Πηγή 2), Οπτικά Προκλητά Δυναμικά (ΟΠΔ) ( Πηγή 3) και Οσφυονωτιαία Παρακέντηση (ΟΝΠ)
Κλινική πορεία - Επιπλοκές
Η νόσος μπορεί να εξελίσσεται με ώσεις (δηλ. να υπάρχουν περίοδοι ασθενείας και περίοδοι φαινομενικής ίασης) ή με προοδευτική επιδείνωση της συμπτωματολογίας στην πάροδο του χρόνου.
Οι σοβαρές και επαναλαμβανόμενες βλάβες της μυελίνης με την πάροδο του χρόνου αφήνουν μόνιμη συμπτωματολογία η οποία πιο συχνά συνίστανται σε δυσαρθρία, τρόμο, νυσταγμό, παρέσεις άκρων, σπαστικότητα, διαταραχές ούρησης.
Επίσης λόγω του ότι πολύ συχνά βλάπτεται το οπτικό νεύρο (οπισθοβολβική νευρίτις) συνυπάρχουν διαταραχές από την όραση. Ακόμη, ο παρατεταμένος κλινοστατισμός και η πτωχή κινητικότητα μπορούν να οδηγήσουν σε επιπλοκές και για τον λόγο αυτό συνιστάται φυσιοθεραπευτική αγωγή.
Θεραπεία
Η θεραπευτική αγωγή βασίζεται σε σκευάσματα που δρουν στο ανοσοποιητικό σύστημα και κυρίως η ιντερφερόνη β και η κοπαξόνη. Πιστεύεται ότι η ιντερφερόνη β και η κοπαξόνη δρουν ανοσορυθμιστικά μειώνοντας την ένταση της αυτοάνοσης αντίδρασης.
Κατ' αυτόν τον τρόπο οι ώσεις του ασθενούς είναι αραιώτερες χρονικά και με μικρόετερη κλινική βαρύτητα.
Επίσης, χρησιμοποιούνται ανοσοκατασταλτικά φάρμακα όπως η κορτιζόνη και κυτταροστατικά.
Το πιο πρόσφατο φάρμακο για την ΣΚΠ λέγεται tysabri ( natalizumab ). Πρόκειται για ένα μονοκλωνικό αντίσωμα το οποίο παρεμποδίζει την είσοδο των λευκοκυττάρων στον εγκέφαλο και κατά συνέπεια μειώνει την φλεγμονή και την βλάβη του εγκεφάλου.
Το tysabri ενδείκνειται σε ασθενείς με υποτροπιάζουσα μορφή της ΣΚΠ και συνιστάται σε εκείνους όπου οι υπάρχουσες θεραπευτικές αγωγές απέβησαν ανεπαρκείς ή μη ανεκτές.
Η αποτελεσματικότητά του, όσον αφορά τις βλάβες στην μαγνητική τομογραφία και την συχνότητα και βαρυτητα των ώσεων, φαίνεται να είναι σχεδόν διπλάσια από εκείνη των ιντερφερονών και της κοπαξόνης.
Παρ’ όλ’ αυτά η χορήγηση του φαρμάκου απαιτεί προσοχή κυρίως γιατί έχουν αναφερθεί σπάνιες περιπτώσεις ‘προιούσας πολυεστιακής λευκοεγκεφαλοπάθειας’ η οποία μπορεί να αποβεί θανατηφόρα. Πάντως με την σωστή χρήση του φαρμάκου η πιθανότητα αυτή εκμηδενίζεται.
Όμως παραμένει πάντα ο κίνδυνος αλλεργικής αντίδρασης (όπως άλλωστε με όλα τα βιολογικά φάρμακα - αντισώματα) και για τον λόγο αυτό η χορήγηση του φαρμάκου πρέπει να γίνεται σε κλινική με ιατρική παρακολούθηση για μια τουλάχιστον ώρα μετά την έγχυση.
Η διαδικασία αυτή θα πρέπει να γίνεται κάθε τέσσερις εβδομάδες.
Σημαντική είναι η ψυχολογική υποστήριξη του ασθενούς (από Ψυχολόγο ή/και με αντικαταθλιπτικά φάρμακα) εφ΄όσον η κακή λειτουργία του ανοσοποιητικού συστήματος υποβοηθείται από μια κακή ψυχολογική διάθεση.
Ακόμη, συνιστάται φυσική αποκατάσταση.
Τέλος, η θεραπεία των συμπτωμάτων της νόσου αποσκοπεί στην όσο το δυνατόν καλλίτερη ανακούφιση του ασθενούς και για τον λόγο αυτό χρησιμοποιούνται αναλγητικά, σπασμολυτικά κ.α. φάρμακα ανάλογα με την περίπτωση.
Πρόληψη
Δεδομένου ότι η αιτιολογία της νόσου παραμένει άγνωστη δεν υπάρχουν συγκεκριμένες συμβουλές για την πρόληψή της.
Περισσότερες πληροφορίες
Για την ορθότερη αντιμετώπιση του προβλήματος που σας απασχολεί θα είναι σκόπιμο να απευθυνθείτε σε ιατρό Νευρολόγο δεδομένου ότι ο κάθε ασθενής αποτελεί ξεχωριστή περίπτωση σε σύγκριση με τους άλλους με την ίδια πάθηση (π.χ.
διαφορετική βαρύτητα και κλινική πορεία).
Ο συγγραφέας του άρθρου παραμένει στην διάθεσή σας για περισσότερες πληροφορίες στην διεύθυνση gkmpa@yahoo.it. Επίσης, μπορείτε να επισκεφτείτε το ιστολόγιο: neyrologia.blogspot.com
Η βαρύτητα και η κλινική πορεία της νόσου διαφέρουν σημαντικά από ασθενή σε ασθενή.
Η θεραπευτική αγωγή βασίζεται κυρίως σε ανοσοκατασταλτικά - ανοσοτροποποιητικά φάρμακα, ψυχολογική υποστήριξη και φυσική αποκατάσταση.
Αιτιολογία
Η αιτιολογία της νόσου είναι άγνωστη. Τα έως τώρα επιστημονικά δεδομένα οδηγούν στο συμπέρασμα ότι πρόκειται για μια διαταραχή του ανοσοποιητικού συστήματος το οποίο πιθανόν αντιδρά ανώμαλα στην προσπάθειά του να εξουδετερώσει κάποιον εξωτερικό παράγοντα.
Πιθανολογείται ότι ο παράγοντας αυτός είναι ένας ή περισσότεροι ιοί.
Παθογένεια
Πρόκειται για μια αυτοάνοση διαταραχή που έχει σαν τελικό αποτέλεσμα την δημιουργία αντισωμάτων ενάντια στην βασική πρωτεΐνη της μυελίνης του ΚΝΣ.
Τα αυτοαντισώματα αυτά δεν καταστρέφουν το σύνολο της μυελίνης του ΚΝΣ αλλά συγκεκριμένες περιοχές κάθε φορά, οι οποίες ονομάζονται εστίες ή πλάκες απομυελίνωσης.
Δεδομένου ότι η μυελίνη στο ΚΝΣ παίζει ουσιαστικό ρόλο στην μετάδοση της πληροφορίας από τον ένα νευρώνα στον άλλο (Πηγή 1), η καταστροφή της προκαλεί διακοπή της επικοινωνίας των διαφόρων τμημάτων του ΚΝΣ με αποτέλεσμα την δυσχερή λειτουργία του.
Κλινική εικόνα - Συμπτώματα
Η συμπτωματολογία της ΣΚΠ (σκλήρυνσης κατά πλάκας) διαφέρει από ασθενή σε ασθενή, αλλά μπορεί να διαφέρει και από ώση σε ώση του ίδιου ασθενούς.
Εξαρτάται από την περιοχή όπου προέκυψε η εστιακή βλάβη της μυελίνης.
Π.χ. αν η βλάβη αυτή αφορά τις αισθητικές οδούς, η συμπτωματολογία θα είναι αιμωδίες (μουδιάσματα), παραισθησίες (μυρμηγκιάσματα). Αν αφορά τις κινητικές οδούς τότε θα έχουμε σαν αποτέλεσμα μείωση ή κατάργηση της μυϊκής ισχύος του ασθενούς (πάρεση ή παράλυση).
Βέβαια, η βλάβη μπορεί να αφορά και οποιαδήποτε άλλη ανατομική δομή του ΚΝΣ με συμπτωματολογία ανάλογη της λειτουργίας του κάθε ανατομικού σχηματισμού. Π.χ. αν η βλάβη αφορά την παρεγκεφαλίδα τότε θα έχουμε δυσαρθρία, αστάθεια βάδισης, ασυνεργία κινήσεων κ.α.
Επίσης, η κλινική εικόνα μπορεί να διαφέρει από ασθενή σε ασθενή. Διακρίνουμε τις περιπτώσεις όπου η νόσος εξελίσσεται με ώσεις ενώ στα μεσοδιαστήματα ο ασθενής είναι φαινομενικά υγιής. Αντίθετα σε άλλες περιπτώσεις εγκαθίσταται μία συμπτωματολογία η οποία επιδεινώνεται με το πέρασμα του χρόνου (προϊούσα μορφή).
Τέλος, συχνή είναι η προσβολή του οπτικού νεύρου με αποτέλεσμα θάμβος οράσεως (οπισθοβολική νευρίτις).
Διάγνωση
Βέβαια, ένας ασθενής που περιγράφει ένα ή περισσότερα από τα ανωτέρω συμπτώματα δεν πάσχει αναγκαστικά από ΣΚΠ. Η συμπτωματολογία εστιακής βλάβης του ΚΝΣ μπορεί να οφείλεται σε διάφορες άλλες αιτίες που προκαλούν βλάβη σε κάποιο σημείο του ΚΝΣ.
Μερικά από αυτά τα αίτια είναι: όγκοι, αγγειακά επεισόδια, αποστήματα, φλεγμονώδεις παθήσεις και απομυελινώσεις άλλης αιτιολογίας.
Επίσης, μπορεί το αναφερόμενο σύμπτωμα να οφείλεται σε άλλου είδους διαταραχή και όχι σε εστιακή βλάβη.
Π.χ. ένας ασθενής που αναφέρει αιμωδίες άνω άκρων μπορεί να πάσχει από νευροφυτικές διαταραχές, σύνδρομο καρπιαίου σωλήνα, περιφερική νευροπάθεια κ.α.
Για τον λόγο αυτό η διάγνωση της ΣΚΠ τίθεται από ειδικούς γιατρούς (Νευρολόγους) με βάση συγκεκριμένα κριτήρια τα οποία είναι κατ' εξοχήν κλινικά (χρησιμοποιούνται ευρέως τα κριτήρια του Poser)( Πηγή 4) αλλά και εργαστηριακά (κυρίως Μαγνητική Τομογραφία Εγκεφάλου ή Σπονδυλικής Στήλης ( Πηγή 2), Οπτικά Προκλητά Δυναμικά (ΟΠΔ) ( Πηγή 3) και Οσφυονωτιαία Παρακέντηση (ΟΝΠ)
Κλινική πορεία - Επιπλοκές
Η νόσος μπορεί να εξελίσσεται με ώσεις (δηλ. να υπάρχουν περίοδοι ασθενείας και περίοδοι φαινομενικής ίασης) ή με προοδευτική επιδείνωση της συμπτωματολογίας στην πάροδο του χρόνου.
Οι σοβαρές και επαναλαμβανόμενες βλάβες της μυελίνης με την πάροδο του χρόνου αφήνουν μόνιμη συμπτωματολογία η οποία πιο συχνά συνίστανται σε δυσαρθρία, τρόμο, νυσταγμό, παρέσεις άκρων, σπαστικότητα, διαταραχές ούρησης.
Επίσης λόγω του ότι πολύ συχνά βλάπτεται το οπτικό νεύρο (οπισθοβολβική νευρίτις) συνυπάρχουν διαταραχές από την όραση. Ακόμη, ο παρατεταμένος κλινοστατισμός και η πτωχή κινητικότητα μπορούν να οδηγήσουν σε επιπλοκές και για τον λόγο αυτό συνιστάται φυσιοθεραπευτική αγωγή.
Θεραπεία
Η θεραπευτική αγωγή βασίζεται σε σκευάσματα που δρουν στο ανοσοποιητικό σύστημα και κυρίως η ιντερφερόνη β και η κοπαξόνη. Πιστεύεται ότι η ιντερφερόνη β και η κοπαξόνη δρουν ανοσορυθμιστικά μειώνοντας την ένταση της αυτοάνοσης αντίδρασης.
Κατ' αυτόν τον τρόπο οι ώσεις του ασθενούς είναι αραιώτερες χρονικά και με μικρόετερη κλινική βαρύτητα.
Επίσης, χρησιμοποιούνται ανοσοκατασταλτικά φάρμακα όπως η κορτιζόνη και κυτταροστατικά.
Το πιο πρόσφατο φάρμακο για την ΣΚΠ λέγεται tysabri ( natalizumab ). Πρόκειται για ένα μονοκλωνικό αντίσωμα το οποίο παρεμποδίζει την είσοδο των λευκοκυττάρων στον εγκέφαλο και κατά συνέπεια μειώνει την φλεγμονή και την βλάβη του εγκεφάλου.
Το tysabri ενδείκνειται σε ασθενείς με υποτροπιάζουσα μορφή της ΣΚΠ και συνιστάται σε εκείνους όπου οι υπάρχουσες θεραπευτικές αγωγές απέβησαν ανεπαρκείς ή μη ανεκτές.
Η αποτελεσματικότητά του, όσον αφορά τις βλάβες στην μαγνητική τομογραφία και την συχνότητα και βαρυτητα των ώσεων, φαίνεται να είναι σχεδόν διπλάσια από εκείνη των ιντερφερονών και της κοπαξόνης.
Παρ’ όλ’ αυτά η χορήγηση του φαρμάκου απαιτεί προσοχή κυρίως γιατί έχουν αναφερθεί σπάνιες περιπτώσεις ‘προιούσας πολυεστιακής λευκοεγκεφαλοπάθειας’ η οποία μπορεί να αποβεί θανατηφόρα. Πάντως με την σωστή χρήση του φαρμάκου η πιθανότητα αυτή εκμηδενίζεται.
Όμως παραμένει πάντα ο κίνδυνος αλλεργικής αντίδρασης (όπως άλλωστε με όλα τα βιολογικά φάρμακα - αντισώματα) και για τον λόγο αυτό η χορήγηση του φαρμάκου πρέπει να γίνεται σε κλινική με ιατρική παρακολούθηση για μια τουλάχιστον ώρα μετά την έγχυση.
Η διαδικασία αυτή θα πρέπει να γίνεται κάθε τέσσερις εβδομάδες.
Σημαντική είναι η ψυχολογική υποστήριξη του ασθενούς (από Ψυχολόγο ή/και με αντικαταθλιπτικά φάρμακα) εφ΄όσον η κακή λειτουργία του ανοσοποιητικού συστήματος υποβοηθείται από μια κακή ψυχολογική διάθεση.
Ακόμη, συνιστάται φυσική αποκατάσταση.
Τέλος, η θεραπεία των συμπτωμάτων της νόσου αποσκοπεί στην όσο το δυνατόν καλλίτερη ανακούφιση του ασθενούς και για τον λόγο αυτό χρησιμοποιούνται αναλγητικά, σπασμολυτικά κ.α. φάρμακα ανάλογα με την περίπτωση.
Πρόληψη
Δεδομένου ότι η αιτιολογία της νόσου παραμένει άγνωστη δεν υπάρχουν συγκεκριμένες συμβουλές για την πρόληψή της.
Περισσότερες πληροφορίες
Για την ορθότερη αντιμετώπιση του προβλήματος που σας απασχολεί θα είναι σκόπιμο να απευθυνθείτε σε ιατρό Νευρολόγο δεδομένου ότι ο κάθε ασθενής αποτελεί ξεχωριστή περίπτωση σε σύγκριση με τους άλλους με την ίδια πάθηση (π.χ.
διαφορετική βαρύτητα και κλινική πορεία).
Ο συγγραφέας του άρθρου παραμένει στην διάθεσή σας για περισσότερες πληροφορίες στην διεύθυνση gkmpa@yahoo.it. Επίσης, μπορείτε να επισκεφτείτε το ιστολόγιο: neyrologia.blogspot.com
Πηγές:
Βιβλιογραφία
1. Γ. Καπαρός. Ειδική Νευροφυσιολογία ΤΕΙ Αθηνών 1999
2. Γ. Καπαρός, Ευθυμίου Α., Κραβαρίτης Δ., Μπαλάκας Ν. Η αξία της
μαγνητικής τομογραφίας στην διάγνωση της σκλήρυνσης κατά πλάκας.
Εργασίας Εαρινής 12ης Συνάντησης Ελλήνων Νευρολόγων. Ιωάννινα: Ελληνική
Νευρολογική Εταιρία, 1996
3. Ε. Κούτρα, Γ. Καπαρός, Δ. Καράκαλος, Ν. Μπαλάκας. Η σημασία της
μεταξύ των δύο οφθαλμών διαφοράς των διακυμματικών χρόνων Ν70-Ν135 σε
ασθενείς με κατά πλάκας σκλήρυνση και φυσιολογικούς λανθάνοντες χρόνους
Ρ100. Εργασίες συνεδρίου Ελληνικής Εταιρείας Ηλεκτροεγκεφαλογραφίας και
Κλινικής Νευροφυσιολογίας. Ναύπλιο: Ελληνική Εταιρεία
Ηλεκτροεγκεφαλογραφίας και Κλινικής Νευροφυσιολογίας, 1994.
4. Poser CM, Patty DW, Scheingerg L et al. New diagnostic criteria for
MS: guidelines for research protocols. Ann Neurology 1983, 13:227-231
Internet
www.nmss.org
www.msif.org
www.greekmssociety.gr